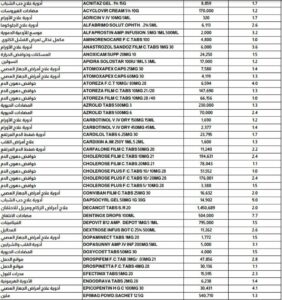
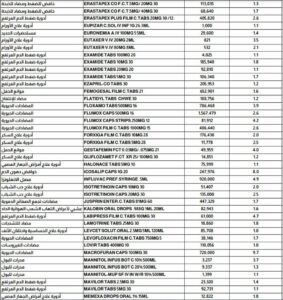
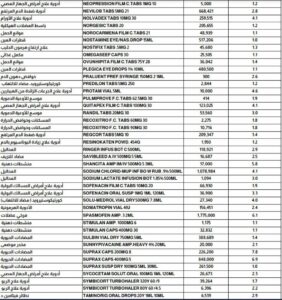
أعلنت هيئة الدواء المصرية، ضخ كميات إضافية من العديد من المستحضرات الدوائية المهمة أبرزها أدوية الضغط والقلب والأورام والمضادات الحيوية.
وأفاد بيان صادر عن الهيئة، يوم الاثنين، بأن الأصناف تتضمن مجموعات علاجية متعددة، على سبيل المثال: (FORXIGA FILM C.TABS 10MG , VASCON DROPS 1% 15ML, SUPRAX CAPS 400MG , NEVILOB TABS 5MG 21, FLATIDYL TABS).
يأتي هذا في وقت تعاني فيه سوق الدواء المصرية، من عدة مشكلات أهمها ارتفاع أسعار الصرف ما أدى لنقص في عدة أدوية ومستحضرات من الصيدليات.